![]() 《初识酸和碱》测试题
《初识酸和碱》测试题
1、单选题
1.除去下列物质中的杂质(括号内是杂质)的操作办法正确的是()
选项 | 物质 | 操作办法 |
A | Fe(Fe2O3) | 加入过量稀盐酸,充分反应后过滤 |
B | CO2 (CO) | 点燃气体 |
C | NaOH溶液[(Ca(OH)2溶液] | 通入过量CO2气体,充分反应后过滤 |
D | CuSO4溶液(硫酸) | 加入过量CuO粉末,加热,充分反应后过滤 |
A.A B.B C.C D.D
2.下列各组物质在溶液中相互之间不反应的是()
A.Ca(OH)2、HNO3、BaCl2 B.Na2SO4、MgCl2、KOH
C.Na2CO3、K2SO4、HCl D.H2SO4、NaCl、Cu(NO3)2
3.下列说法正确的是( )
A.氢氧化钠固体久置于表面皿上,没有明显现象
B.硝酸铵固体溶于水后,溶液的温度几乎不变
C.小木棍蘸取浓硫酸一段时间后,小木棍变黑
D.细铁丝伸入盛有氧气的集气瓶中,剧烈燃烧,火星四射,生成黑色固体
4.下列各组离子在pH=11的水溶液中能很多共存的是()
A.NH4+、NO3﹣、K+、SO42﹣ B.Mg2+、CI﹣、Na+、NO3﹣
C.Ba2+、CO32﹣、H+、Cl﹣ D.K+、CO32﹣、NO3﹣、Na+
5.下列有关实验操作的叙述正确的是
①用广泛 pH 试纸测定某溶液的 pH 值为 5.6
②用 10mL 量筒量取 8.8mL 水
③蒸发结束用玻璃棒将食盐转移到指定容器中
④稀释浓硫酸时将水沿着烧杯壁慢慢注入浓硫酸中,并用玻璃棒不断搅拌
A.①②③ B.②③④ C.①④ D.②③
6.剖析推理是化学学习中常见的思维办法,下列推理正确的是()
A.由于燃烧需要同时满足三个条件,所以灭火也要同时除去这三个条件
B.中和反应有盐和水生成,所以有盐和水生成的反应肯定是中和反应
C.可燃气体与空气混合点燃可能爆炸,所以CO与空气混合点燃时或许会爆炸
D.分子、原子都是不显电性的粒子,所以不显电性的粒子肯定是分子或原子
7.下列说法正确的是()
A.生成盐和水的反应肯定是中和反应
B.将硝酸铵固体溶于水溶液温度会升高
C.现在计入空气污染指数的有害气体包含:SO2、NO2、CO2、CO等
D.稀盐酸、稀硫酸化学性质相似,是由于其溶液中都含有H+
8.下列实验操作正确的是( )
A.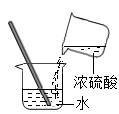 稀释浓硫酸 B.
稀释浓硫酸 B.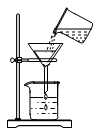 浊液过滤 C.
浊液过滤 C.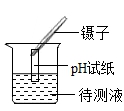 定溶液的pH D.
定溶液的pH D.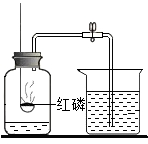 测空气中氧气的含量
测空气中氧气的含量
9.关于家里一些食品及生活用品的 pH(如图),说法正确的是

A.牙膏是中性物质
B.酱油显碱性
C.食醋的酸性比葡萄汁强
D.胃酸过多的人宜多吃葡萄
10.物质存放在敞口烧杯中一段时间后,水平变大且变质的是
①浓盐酸 ②浓硫酸 ③烧碱 ④食盐 ⑤生石灰 ⑥稀硫酸
A.①⑥ B.②③⑤
C.③⑤ D.②④⑤
11.推理是化学学习中常见的思维办法,下列推理正确的是( )
A.中和反应生成盐和水,所以生成盐和水的反应肯定是中和反应
B.溶液是均一稳定的,所以均一稳定的物质肯定是溶液
C.离子是带电荷的粒子,带电荷的粒子肯定是离子
D.碱性溶液能使无色酚酞试液变红,能使无色酚酞试液变红的溶液肯定是碱性溶液
12.化学实验操作的规范性、安全性是实验成败的关継。下列如图所示的实验操作正确的是
A.过滤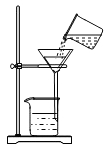 B.蒸发结晶
B.蒸发结晶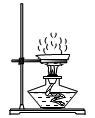
C.测定溶液的pH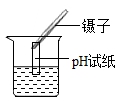 D.稀释浓硫酸
D.稀释浓硫酸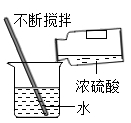
13.厨房中的下列物质或其水溶液呈酸性的是()
A.食醋 B.淀粉 C.白糖 D.豆油
2、实验题
14.实验室提供下列药品:碳酸钠固体、块状大理石、粉末状大理石、稀硫酸、稀盐酸和浓盐酸;A、B、C、D、E、F、G、H等装置和试管等仪器.
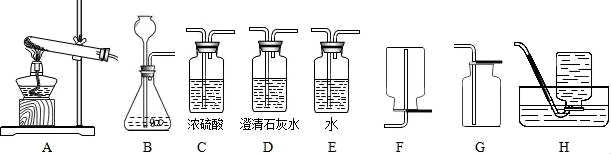
(1)制取CO2的发生装置选_____(填序号),按需要连接好装置后,在装入药品之前必不可少的操作_____.制CO2的装置还可以用来制取_____气体,其反应原理是:_____(用化学方程式表示).将装置A和装置H连接可制取大家容易见到的_____气体.
(2)检验二氧化碳的办法用化学方程式表示为_____.
(3)在四支试管中取等量固体和稀硫酸、稀盐酸反应,现象如表.
反应物 | ①粉末状大理石 +稀盐酸 | ②碳酸钠固体 +稀硫酸 | ③块状大理石 +稀盐酸 | ④块状大理石 +稀硫酸 |
现 象 | 剧烈,瞬间完成 | 剧烈,瞬间完成 | 有平稳气流产生 | 非常慢,稍后停止 |
由此推知,实验室用于制取CO2的药品最适当的是_____(填序号);该反应的反应方程式为:_____.
(4)若要制取干燥的CO2,所有装置的连接顺序为_____.
(5)若不慎用浓盐酸代替稀盐酸制得了CO2气体,要得到纯净干燥的CO2,所有装置的连接顺序为_____.
3、判断题
15.某工厂甲乙两车间排放的废水,分别含有以下五种物质:硫酸镁、硫酸铜、氢氧化钠、氯化铁、氯化钡中的3种和2种,且甲、乙两车间各自的废水中均无沉淀物.若将两车间的废水按适合的比率混合,生成4种沉淀,其中三种是氢氧化物.沉淀收购后,排放出同一种钠盐的稀溶液.试判断:
(1)甲车间的废水中含有些3种物质是_____、_____、_____,乙车间含有些_____、_____;
(2)有关的化学方程式_____.
16.A~F是碳单质、氧化铜、二氧化碳、稀硫酸、氢氧化钠和碳酸钠六种物质中的某一种,A、B都是黑色固体,E是盐,它们之间的相互关系如图所示。请回答下列问题:
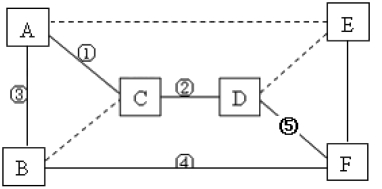
C的化学式是__________。
B与F反应的化学方程式为________。
E与F反应的化学方程式为_______。
上图关系中________的反应是中和反应。
在上图中,三个虚线连接中存在转化关系的有:____→___;___→____。
17.概括是学化学的要紧办法,在学习H2SO4与Ca(OH)2溶液的化学性质时构建了如下常识互联网图,A、B、C、D是不相同种类别的化合物,D是胃液的主要成分,“﹣”表示相连的物质在肯定条件下可以发生化学反应。
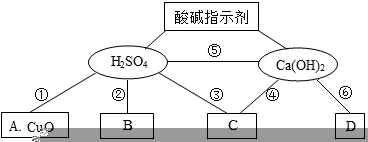
(1)小红同学将紫色石蕊试液滴入Ca(OH)2溶液中,溶液变为_____色。若要测定C物质的酸碱性,应选择_____(填序号)。
①pH试纸 ②石蕊试液 ③酚酞试液
(2)写出B物质的类别_____(填单质、氧化物、酸、碱、盐)。
(3)写出图中是中和反应的是_____(填编号)。
(4)写出反应①的化学方程式为_____,写出符合反应④化学方程式_____。
4、计算题
18.某同学在做完木炭还原氧化铜的实验后,想对反应后固体中是不是含有氧化铜进行探究,为此他进行了如图所示的实验。请计算:
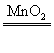
(1)混合物中氧化铜的水平为_____g。
(2)所用稀盐酸中溶质的水平分数_____(计算结果精准到0.1%)。
19.在实验室中,小明发现了一瓶氢氧化钙粉末试剂瓶盖有破损,取部分粉末作为样品对其变质状况进行剖析,实验室温度20℃查阅氢氧化钙的溶解度并进行如下实验。
氢氧化钙溶解度表
温度℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
溶解度g | 0.185 | 0.176 | 0.165 | 0.153 | 0.141 | 0.138 | 0.116 | 0.106 |
(1)取1g样品溶于100g水中,出现浑浊现象。小明觉得该固体己经变质。你感觉这种说法是不是正确?______(填“正确”或“不正确”)。理由是:______。
(2)小明另取2g样品于大烧杯中,加足量水充分溶解配制成1850g溶液,并通入CO2.溶液的水平与反应的CO2水平关系如图所示。请计算:该样品中氢氧化钙的水平分数______。
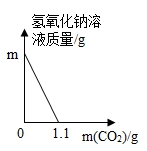
(3)配制的氢氧化钙溶液浓度为______。
参考答案
1.D 2.D 3.C 4.D 5.D 6.C 7.D 8.D 9.C 10.C 11.D 12.D 13.A
14.B 检查装置的气密性 氧气或氢气 2H2O2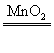 2H2O+O2↑(或Zn+H2SO4=ZnSO4+H2↑) 氧气 Ca(OH)2+CO2═CaCO3↓+H2O ③ CaCO3+2HCl═CaCl2+CO2↑+H2O BCG BECG
2H2O+O2↑(或Zn+H2SO4=ZnSO4+H2↑) 氧气 Ca(OH)2+CO2═CaCO3↓+H2O ③ CaCO3+2HCl═CaCl2+CO2↑+H2O BCG BECG
15.MgSO4 CuSO4 FeCl3 NaOH BaCl2 MgSO4+2NaOH═Mg(OH)2↓+Na2SO4;CuSO4+2NaOH═Cu(OH)2↓+Na2SO4;FeCl3+3NaOH═Fe(OH)3↓+2NaCl;MgSO4+BaCl2═BaSO4↓+MgCl2
16.CO2 ![]()
![]() ⑤ CuO CO2 NaOH Na2CO3
⑤ CuO CO2 NaOH Na2CO3
17.蓝; ①② 碱 ② CuO+H2SO4═CuSO4+H2O; Na2CO3+Ca(OH)2═CaCO3↓+2NaOH
18.2 6.1%
19.不正确 由于氢氧化钙的溶解度非常小,致使不可以完全溶液而浑浊 92.5% 0.1%







