![]() 《常见的金属和盐》测试题
《常见的金属和盐》测试题
1、单选题
1.实验室中区别下列各组物质的两种办法都正确的是()
选项 | 需区别的物质 | 办法 | 办法 |
A | 海水和自来水 | 尝味道 | 测试导电性 |
B | 硝酸铵和磷矿粉 | 察看颜色 | 加熟石灰研磨,闻气味 |
C | 棉织品和涤纶织品 | 察看颜色 | 点燃闻气味 |
D | 氮气和二氧化碳 | 分别伸入燃着的木条 | 分別通入紫色石溶液 |
A.A B.B C.C D.D
2.“民以食为天”,食品安全无小事。下列有关食品安全的常识正确的是()
A.亚硝酸钠有咸味,可替代食盐做调味品
B.常见的食品塑料袋多为聚乙烯塑料袋
C.熟石灰可以做食品干燥剂
D.农药本身有毒,应该禁止施用农药
3.只用一种试剂一次就可将盐酸、氢氧化钠溶液、氯化钡溶液三种物质辨别出来,这种试剂不是( )
A.紫色石蕊溶液 B.硫酸铜溶液 C.硝酸银溶液 D.碳酸钠溶液
4.将等水平的镁、铁、锌,分别放入三份水平分数相同的稀盐酸中,反应生成的氢风韵量与反应时间的关系如图所示。依据图中信息,下列判断不正确的是()
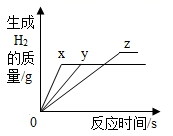
A.图线X表示镁的反应状况 B.铁消耗稀盐酸的水平最大
C.锌肯定过量 D.镁肯定过量
5.下列实验策略不可以达到实验目的的是
选项 | 实验目的 | 实验策略 |
A | 比较铁、铜的金属活动性强弱 | 将铁、铜分别放入硫酸锌溶液中,察看现象 |
B | 区别NaOH和NH4NO3固体 | 加水溶解,察看 |
C | 区别氢气和一氧化碳 | 分别点燃两种气体,检验燃烧产物 |
D | 除去N2中O2 | 通过灼热的铜网 |
A.A B.B C.C D.D
6.向肯定水平含BaCl2和HCl的混合溶液中逐滴加入溶质水平分数为10%的Na2 CO3溶液,反应过程中加入的Na2CO3溶液的水平与产生沉淀或气体的水平关系如图所示,下列说法不正确的是( )
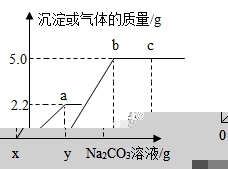
A.图中Oa段表示产生气体的过程且X的值为53
B.图中Xb段表示产生沉淀的过程且Y值为63.6
C.C点时,溶液的pH>7(不考虑气体的溶解)
D.b点时,溶液中的溶质有1种
7.物质的作用与性质密切有关。下列说法不正确是
A.铁制品表面涂“银粉”防生锈,是由于铝的化学性质比铁稳定
B.二氧化碳用于灭火,是由于二氧化碳不可燃、不助燃且密度比空气大
C.氮气常用作保护气,是由于氮气的化学性质不活泼
D.炼铁高炉的炉渣出口比生铁出口高,是由于炉渣的密度比生铁小
8.为达到实验目的,下列实验策略或结论不正确的是()
选项 | 实验目的 | 实验策略或结论 |
A | 检验某固体为碳酸盐 | 取样,滴加盐酸,察看是不是有气泡 |
B | 辨别①CuSO4溶液②稀H2SO4③NaCl溶液④NaOH溶液 | 不需要其它任何试剂就能辨别,且辨别出的顺序为①④②③或①④③② |
C | 除去氯化钙溶液中少量稀盐酸 | 加入过量的碳酸钙、过滤 |
D | 辨别NaC1溶液、Na2SO4溶液和(NH4)2SO4溶液 | 各取少量于试管中,分别滴加Ba(OH)2溶液,察看现象 |
A.A B.B C.C D.D
9.下表列出了除去物质中所含少量杂质的办法,其中错误的是
| 物质 | 所含杂质 | 除去杂质的办法 |
A | 铜粉 | 铁粉 | 加入过量稀盐酸,过滤,干燥 |
B | NaCl | CaCO3 | 溶解、过滤、蒸发 |
C | Cu 2溶液 | AgNO3 | 加入过量的铜粉,过滤 |
D | NaOH溶液 | Na2CO3 | 加入适当的氯化钙溶液,过滤 |
A.A B.B C.C D.D
10.对于化学反应A+B=C+D的下列说法中,正确的是
A.若C、D分别为盐和水,则该反应肯定是中和反应
B.若A、B、C、D都是化合物,该反应肯定是复分解反应
C.若A为碱溶液,B为盐溶液,则C和D可能是两种沉淀
D.若C、D分别为单质和化合物,则该反应肯定是置换反应
11.推理是化学学习中常见的思维办法。下列推理正确的是()
A.酸能使石蕊试液变红,![]() 也能使紫色的石蕊试液变红,所以
也能使紫色的石蕊试液变红,所以![]() 是酸
是酸
B.饱和溶液不可以继续溶解某种溶质,则饱和溶液也不可以继续溶解其他溶质
C.NaOH溶液中的![]() 能与酸反应,则KOH溶液中的
能与酸反应,则KOH溶液中的![]() 也能与酸反应
也能与酸反应
D.盐是由金属离子和酸根离子组成的,![]() 中没金属离子,不是盐
中没金属离子,不是盐
12.下列物质的名字、俗名与化学式完全对应的是
A.氯化钠 化合物 NaCl B.碳酸氢钠 混合物 NaHCO3
C.氢氧化钙 氧化物 CaO D.氢氧化钠 纯碱 NaOH
13.下列对物质的分类正确的是
A.塑料、涤纶、合成橡胶是合成高分子材料
B.尿素、氨水、碳酸氢钠是氮肥
C.干木头、金属、石墨是导体
D.酱油、黑芝麻糊、蒸馏水是混合物
2、实验题
14.请依据下图回答问题:
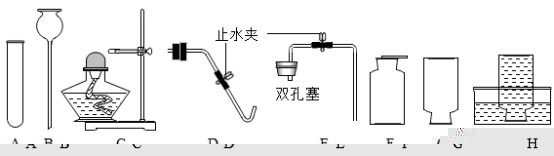
(1)写出下列仪器的名字:A_____,B_____。
(2)用KClO3与MnO2混合制取和采集O2,最好使用上图中的_____(填字母,下同),采集时察看到_____表明O2已集满。上述制取O2反应的化学方程式为_____。
(3)实验室常用硫化亚铁(FeS)固体和稀硫酸溶液,在常温下发生复分解反应制取硫化氢(H2S)气体,其发生装置应使用上图中的_____(加持装置已略去),制取硫化氢气体的化学方程式为_____。
(4)用如图装置可以采集氢气,则气体应从_____(填“a”或“b”)端通入;若气体从a端通入广口瓶干燥氢气,广口瓶应盛装试剂的名字是_____。

(5)兴趣小组在探究CO2性质实验时进行了如图改进,将左边胶头滴管中的稀硫酸注入装有碳酸钠粉末的小试管中,右边管内挂的是紫色石蕊试液浸泡过的滤纸条,其中一条是湿润的,一条是干燥的。

①证明二氧化碳可与水反应的现象是_____。
②将右边胶头滴管内的药品注入U形管内,察看到气球明显变瘪,则右边胶头滴管中的药品为_____。
3、判断题
15.如图中A—G为初中化学中容易见到物质,其中A、B、D是由两种元素组成的物质,且A、B所含元素类型相同;F可用于改良酸性土壤。它们之间的关系如下图所示(“—”表示相连两物质之间能发生反应,“→”表示由某一物质转化为另一物质,部分反应物生成物及反应条件己略去),每一个虚线圈中各反应的基本反应种类相同。
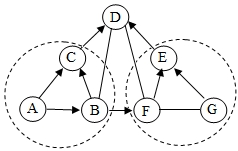
(1)写出物质的化学式:B_____;F_____。
(2)反应G→E的基本反应种类是_____。
(3)反应F—G的化学方程式是_____。
(4)实验室用A制取C的化学方程式是_____。
16.现欲探究一固体混合物 A的成分,已知其中可能含有NH4NO3、NaCl、BaCO3、Cu(NO3)2四种物质中的两种或多种。按下述步骤进行实验探究,察看实验现象,并加以剖析推理(设过程中所有发生的反应都恰好完全反应)
I.取肯定水平的该固体混合物A放入一洁净烧杯中,向其中加入足量水,搅拌,待烧杯中物质充分混合后,过滤,得白色沉淀B和蓝色滤液C.
II向步骤I所得滤液C中滴加适当氢氧化钠溶液,出现的现象如图中所述:
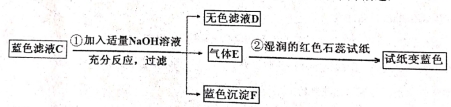
试依据实验过程和发生的现象判断:
(1)白色沉淀B是____________(写化学式)。
(2)固体混合物A中肯定存在的物质是____________(写化学式)。
(3)写出实验过程①中生成蓝色沉淀F的化学方程式______________________。
(4)滤液D中肯定很多存在的酸根离子为__________(写离子符号)。
(5)若要检验混合物A中不可以确定的物质是不是存在,可以用无色滤液D进一步实验,请简述实验操作步骤,发生的现象及结论:________________。
17.物质世界中的六个部落举行“六方谈判”。六个部落的谈判代表A~F分别是稀硫酸、水、生石灰、氢氧化钙、碳酸钠、二氧化碳六种物质中的一种。地方的安排规则是相邻的代表之间能发生化学反应,如图所示。其中A、B都是氧化物,F是气体。请回答下列问题:

B的化学式是_____,
C物质的作用为_____,
D一E之间反应的化学方程式为_____,
A、B之间的反应的基本种类是_____。
4、计算题
18.小黄同学为了测定某Cu﹣Ag合金中各金属的含量,取这种合金4.8 g与AgNO3溶液反应,加入AgNO3溶液的水平m与充分反应后所得固体的水平b的关系如图所示.请计算:

(1)AgNO3溶液中溶质的水平分数(结果精准 至0.1%);
(2)该合金中银和铜的水平比(结果精准至0.1).
19.200克稀硫酸和169.9克的氯化钡溶液恰好完全反应,测得反应后所得溶液的水平为300克。求反应后所得溶液的溶质水平分数。
20.泡腾片配料表如下:
成分 | 柠檬酸 | 碳酸氢钠 | 维生素C | 乳糖 | 色素香精 |
每片含量(4 g/片) | 未知 | 未知 | 0.2 g | 未知 | 极少量 |
泡腾片放入温开水中,浮于水面上,产生很多气泡,所得溶液喝起来酸甜可口。已知:柠檬酸的化学式为C6H8O7,相对分子水平为192;泡腾片溶于水时,碳酸氢钠刚好与柠檬酸完全反应,生成Na3C6H5O7。
(1)泡腾片在水中产生气体的化学式为_____。泡腾片中柠檬酸与碳酸氢钠的水平比为_____。
(2)称取5.00 g泡腾片放入200.00 g温开水中,待泡腾片完全溶解,不再产生气体后,测得溶液水平为203.68 g.通过计算确定泡腾片中柠檬酸的水平分数_____。
参考答案
1.B 2.B 3.C 4.C 5.A 6.B 7.A 8.A 9.D 10.C 11.C 12.A 13.A
14.试管 长颈漏斗 ACDH(漏写不给分) 集气瓶口有气泡冒出 2KClO3![]() 2KCl+3O2↑ ABE(漏写不给分) FeS+H2SO4═H2S↑+FeSO4 b 浓硫酸 干燥的滤纸不变色,湿润的滤纸变红色(漏写不给分) NaOH溶液(合理即可)
2KCl+3O2↑ ABE(漏写不给分) FeS+H2SO4═H2S↑+FeSO4 b 浓硫酸 干燥的滤纸不变色,湿润的滤纸变红色(漏写不给分) NaOH溶液(合理即可)
15.H2O Ca2 复分解反应。 Ca2+Na2CO3=2NaOH+CaCO3↓ 2H2O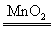 2H2O+O2↑
2H2O+O2↑
16.BaCO3 BaCO3、Cu(NO3)2、NH4NO3 Cu(NO3)2+2NaOH = Cu(OH)2↓+2NaNO3 NO3- 取溶液D少许,向其中加入硝酸银和稀硝酸溶液,若出现白色沉淀,证明有氯化钠,不然没。(只加入硝酸银溶液也可以得满分)
17.CaO 除锈 Ca2+ Na2CO3=CaCO3↓+2NaOH 化合反应
18.(1)12.1%(2)2:
1
19.7.3%
20.CO2 16:21 38.4%







